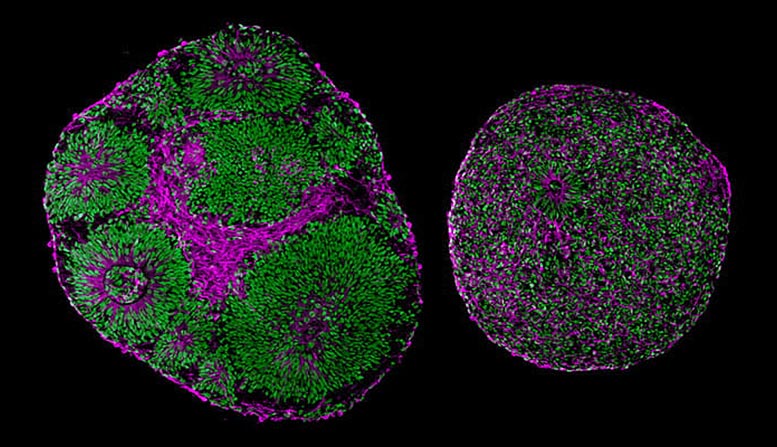
Les micrographies révèlent des différences significatives de taille et de structure entre les organites cérébraux dérivés d’un patient atteint du syndrome de Pitts Hopkins (à droite) et d’un témoin (à gauche). Crédit : Université de Californie, San Diego Health Sciences
L’étude de l’Université de Californie à San Diego (UCSD) utilise des tissus cérébraux humains cultivés en laboratoire pour identifier les anomalies neurologiques du syndrome de Pitt Hopkins et tester des outils de thérapie génique.
Dans une étude publiée le 2 mai 2022 dans la revue Communication NatureDes scientifiques de l’Université de Californie, San Diego School of Medicine, ont utilisé des organoïdes du cerveau humain pour découvrir comment une mutation génétique associée à un autisme sévère perturbe le développement neurologique. L’utilisation d’outils de thérapie génique pour restaurer la fonction des gènes a sauvé avec succès la structure et la fonction neuronales.
Plusieurs maladies neurologiques et neuropsychiatriques, dont les troubles du spectre autistique (TSA) et la schizophrénie, ont été associées à des mutations du facteur de transcription 4 (TCF4), un gène essentiel au développement du cerveau. Les facteurs de transcription régulent le moment où d’autres gènes sont activés ou désactivés, de sorte que leur présence, ou leur absence, peut avoir un effet domino sur le fœtus en développement. Cependant, on ne sait pas grand-chose sur ce qui arrive au cerveau humain lorsque cela se produit TCF4 muté.
Pour explorer cette question, les chercheurs se sont concentrés sur le syndrome de Pitts Hopkins, un trouble du spectre autistique causé par des mutations dans TCF4. Les enfants atteints de la maladie héréditaire ont de profondes déficiences cognitives et motrices et sont généralement non verbaux.
Syndrome de Pitt Hopkins (PTHS) est une maladie génétique rare caractérisée par un retard de développement, une épilepsie, des traits faciaux distinctifs et une hyperventilation potentiellement intermittente suivie d’apnée. Au fur et à mesure que l’on en découvre plus sur Pitt Hopkins, le spectre développemental des troubles s’élargit pour inclure l’autisme, l’anxiété, le TDAH et les troubles sensoriels. Elle est associée à un défaut du chromosome 18, en particulier à l’expression insuffisante du gène TCF4.
Les modèles de souris existants du syndrome de Pitt Hopkins ne parviennent pas à imiter avec précision les caractéristiques neurologiques des patients, de sorte que l’équipe de l’UCSF a créé un modèle de recherche humain pour le trouble. En utilisant la technologie des cellules souches, ils ont transformé les cellules de la peau des patients en cellules souches, qui ont ensuite été développées en organites cérébraux tridimensionnels, ou « mini-cerveaux ».
Les premières observations d’organoïdes cérébraux ont révélé un grand nombre de différences structurelles et fonctionnelles entre TCF4Échantillons mutagènes et leurs témoins.
L’auteur principal de l’étude, Alison R. Mottery, Ph.D., professeur à l’UCSD School of Medicine, directeur du programme de cellules souches de l’UCSD et membre du Consortium de Sanford pour la médecine régénérative, a déclaré.
Le TCF4Les organites mutants étaient beaucoup plus petits que les organites normaux, et de nombreuses cellules n’étaient pas réellement des neurones, mais des progéniteurs neuronaux. Ces cellules simples sont censées proliférer puis devenir des cellules cérébrales spécialisées, mais dans les organites mutés, une partie de ce processus a mal tourné.
Une série d’expériences a révélé que TCF4 Un barrage a entraîné une perturbation du cours de la rivière SOx Les gènes et la voie Wnt, deux signaux moléculaires importants qui guident les cellules embryonnaires pour se multiplier, mûrir en neurones et se déplacer vers le bon site dans le cerveau.
En raison de ce déséquilibre de régulation, les lignées neuronales n’ont pas proliféré efficacement et donc moins de neurones corticaux ont été produits. Les cellules qui avaient déjà mûri en neurones étaient moins excitables que la normale et restaient souvent regroupées plutôt que de s’organiser en circuits neuronaux finement réglés.
Cette structure cellulaire atypique a perturbé le flux d’activité neuronale dans les organites cérébraux mutés, ce qui, selon les auteurs, contribuerait probablement à une altération des fonctions cognitives et motrices.
« Nous avons été surpris de voir des problèmes de développement aussi importants à tous ces différents niveaux, et nous nous sommes demandé ce que nous pouvions faire pour les résoudre », a déclaré le premier auteur Fabio Papez, PhD, professeur agrégé à l’Université de Campinas et chercheur invité à UCLA. . San Diego School of Medicine, qui a supervisé conjointement le travail avec Muotri. Papes a un parent qui souffre du syndrome de Pitts Hopkins, ce qui l’a incité à étudier TCF4.
L’équipe a testé deux stratégies de thérapie génique différentes pour restaurer un gène fonctionnel dans le tissu cérébral. Les deux méthodes ont effectivement augmenté TCF4 Ce faisant, les phénotypes du syndrome de Pitt Hopkins ont été corrigés aux niveaux moléculaire, cellulaire et électrophysiologique.
« Le fait que nous puissions corriger ce gène et que tout le système nerveux se rétablisse, même au niveau fonctionnel, est incroyable », a déclaré Mootri.
Mootri note que ces interventions génétiques se sont produites au stade prénatal du développement du cerveau, alors que dans un cadre clinique, les enfants recevraient leur diagnostic et leur traitement quelques années plus tard. Ainsi, les essais cliniques doivent d’abord confirmer si une intervention ultérieure est toujours sûre et efficace. L’équipe peaufine actuellement des outils de thérapie génique récemment homologués en vue d’un tel essai, dans lequel on espère que l’injection dans le squelette du vecteur génique restaurera la fonction du TCF4 dans le cerveau.
« Pour ces enfants et leurs proches, toute amélioration de la fonction cognitivo-motrice et de la qualité de vie vaut la peine d’être essayée », a déclaré Mootri.
« La chose vraiment spéciale à propos de ce travail est que ces chercheurs vont au-delà du laboratoire et travaillent très dur pour rendre ces découvertes transposables à la clinique », a déclaré Audrey Davido, présidente de la Fondation Pitt Hopkins pour la recherche. « C’est bien plus qu’un excellent article académique; c’est une véritable mesure de ce que la science bien aguerrie peut accomplir dans l’espoir de changer des vies humaines pour le mieux. »
Référence : « La perte du facteur de transcription 4 est associée à des déficits de la prolifération des progéniteurs et du contenu des neurones corticaux » par Fabio Papis, Antonio B. Camargo, Janina S. De Souza, Vinicius MA, Carvalho, Ryan A. Seto, Irene Lamontani, Jose R. Teixeira, Simone H. Avancini, Sandra M. Sanchez Sanchez, Thiago S. Nakahara, Carolina N. Santo, Wei Wu, Hang Yao, Barbara M. P. Araujo, Paolo Enf Filho et Gabriel J. , 2 mai 2022, Communication Nature.
DOI : 10.1038 / s41467-022-29942-w
Les co-auteurs sont : Janina S. de Souza, Ryan A. Sito, Irene Lamontani, Simone H. Avancini, Sandra M. Sanchez Sanchez, Wei Wu, Hang Yao et Gabriel Haddad à l’UCSD ; Antoine B. Camargo, Vinicius MA Carvalho, José R Teixeira, Thiago S. Nakahara, Carolina N Santo, Barbara MB Araujo et Paulo Enf Filho à l’Université de Campinas.
Ce travail a été financé en partie par les National Institutes of Health (subvention R01 MH123828), la Pitts Hopkins Foundation for Research, la São Paulo Research Foundation (subventions 2020/11451-7, 2018/03613-7, 2018/04240-0) et le Joint Genome Institute du ministère de la Santé American Energy (DE-AC02-05CH11231).
Divulgations : Alison R. Mootri est la co-fondatrice de TISMOO, une société dédiée à l’analyse génétique et à l’organogenèse du cerveau humain et détient une participation.

« Évangéliste généraliste de la bière. Pionnier du café depuis toujours. Défenseur certifié de Twitter. Internetaholic. Praticien du voyage. »






More Stories
Une nouvelle recherche révèle que les dinosaures n’étaient pas aussi intelligents qu’on le pensait
Daily Telescope : La nébuleuse de la Tête de Cheval comme nous ne l'avons jamais vue auparavant
Transformer la matière noire invisible en lumière visible